Cu patru zile înainte de a primi nota privind retragerea autorizaţiei de punere pe piaţă a produselor injectabile, Institutul Cantacuzino a fost amendat de ANM cu 20.000 de lei pentru distribuirea în maternităţi a unui vaccin expirat menit să protejeze bebeluşii de tuberculoză.
Producţia a fost sistată pe 8 februarie
 “În urma unui control periodic, care se face la fiecare trei ani, inspectorii ANM au găsit deficienţe critice şi majore la liniile de fabricaţie de la Cantacuzino. S-a luat decizia închiderii acestora, însă deocamdată nu s-a stabilit durata suspendării producţiei. Institutul trebuie să intre într-un proces de retehnologizare”, ne-a declarat farmacistul specialist Anca Crupariu, şefa Serviciului de comunicare din cadrul ANM.
“În urma unui control periodic, care se face la fiecare trei ani, inspectorii ANM au găsit deficienţe critice şi majore la liniile de fabricaţie de la Cantacuzino. S-a luat decizia închiderii acestora, însă deocamdată nu s-a stabilit durata suspendării producţiei. Institutul trebuie să intre într-un proces de retehnologizare”, ne-a declarat farmacistul specialist Anca Crupariu, şefa Serviciului de comunicare din cadrul ANM.
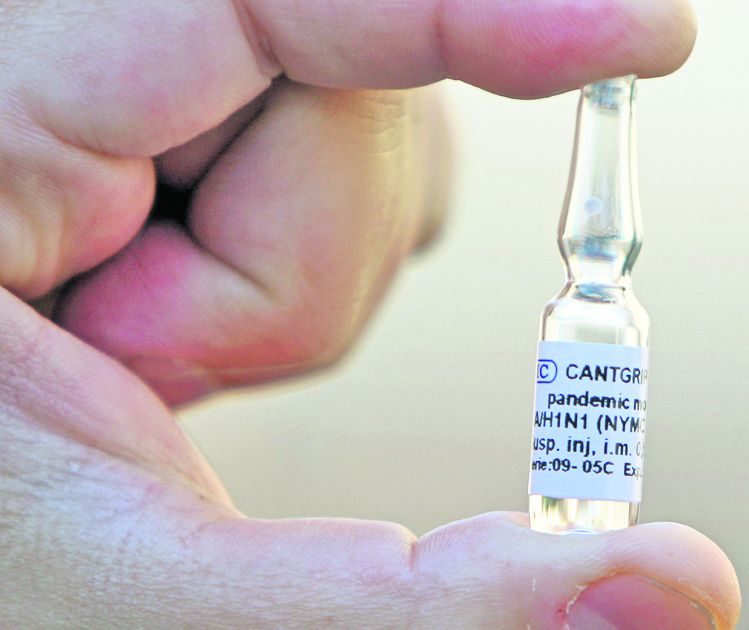
Specialista a recunoscut pentru Libertatea că printre liniile de producţie cu probleme se numără şi cea a vaccinului contra gripei porcine. Cu toate acestea, ea ne-a declarat: “Fiolele deja distribuite sunt în continuare valabile şi pot fi administrate fără probleme”.
Fiolele distribuite rămân valabile
Conform Mediafax, Institutul Cantacuzino a cerut ieri Ministerului Sănătăţii (MS) să îi permită să continue producţia de vaccinuri până la sfârşitul acestui an, timp în care, în paralel, se vor face toate modernizările necesare. Altfel, cei 450 de specialişti care lucrează aici vor rămâne şomeri.

Pentru ca piaţa vaccinurilor să nu fie afectată, producţia ar trebui reluată până în mai. “La Cantacuzino nu se mai produceau oricum vaccinuri în această perioadă, deoarece pentru gripa A(H1N1) s-a oprit producţia după cinci milioane de doze, iar pentru vaccinul BCG (contra tuberculozei – n.r.) e în curs de instalare noua linie tehnologică. În privinţa noului vaccin contra gripei sezoniere, producţia va începe prin luna mai”, a precizat prof. dr. Geza Molnar, consilier MS, pentru NewsIn.
Scandalul, declanşat de un ser pentru bebeluşi
Scandalul a început în ultimele zile ale lunii trecute, de la cele 70.000 de doze de vaccin BCG produse de Institutul Cantacuzino expirate, pentru care iniţial Agenţia Naţională a Medicamentului (ANM) a dat aviz de prelungire cu şase luni a termenului de valabilitate. Ulterior, ANM a trimis un comunicat în care a susţinut că, de fapt, a cerut retragerea tuturor produselor trimise în teritoriu, precizând că a autorizat prelungirea valabilităţii cu şase luni numai pentru vaccinurile fabricate după 22 ianuarie 2010.
70.000 de doze erau expirate
În urmă cu o săptămână, Ministerul Sănătăţii a comunicat sistarea utilizării vaccinului BCG cu termen de valabilitate depăşit, urmând ca imunizarea nou-născuţilor împotriva tuberculozei să fie reluată în aprilie, când va fi gata alt lot de vaccin. Din cele 70.000 de doze expirate au fost retrase doar 64.000, pentru că 6.000 au fost deja utilizate.
Tot Ministerul Sănătăţii susţinea că micuţii vaccinaţi nu vor avea probleme, singura consecinţă a expirării fiind aceea că injecţia nu-şi va face efectul. Vaccinarea BCG trebuia reluată în aprilie când se estima că va fi gata un nou lot produs la Cantacuzino.
Ministerul Sănătăţii a cumpărat 5.000.000 de doze de vaccin antigripal
Până în prezent, peste 1,5 milioane de români s-au vaccinat împotriva gripei porcine. Ministerul Sănătăţii (MS) comandase Institutului Cantacuzino 5 milioane de doze de vaccin antigripal cu tulpină pandemică, pentru care a şi plătit 20 de milioane de lei, echivalentul a aproximativ 5 milioane de euro. Potrivit MS, numărul total de îmbolnăviri cu virusul A(H1N1) a ajuns la 6.998, dintre care 122 au fost fatale.
Situaţia a fost similară în 2005
La sfârşitul anului 2005, conducerea Institutului Cantacuzino recunoştea că este nevoie de o investiţie de patru milioane de euro la fluxurile de producţie. Conform normelor impuse de Comunitatea Europeană, tuturor producătorilor de medicamente li se cerea ca, de la 1 ianuarie 2006, să respecte reguli stricte privind fabricaţia.
E vorba de aşa-numitele GMP-uri, standarde care garantează capacitatea unei companii de a furniza produse de calitate superioară, printr-un sistem performant de management al calităţii. La patru ani de la intrarea în vigoare a normelor, institutul se confruntă cu aceleaşi probleme şi este nevoit să investească pentru a-şi putea relua producţia de produse injectabile.

:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/280_d869ee94813a5a93e6b2e8380642431e.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/280_0aee8c9e4792b530d95e4eda7b0edda1.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/280_48a578eda90e65eb2115f8fa24510554.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/280_2037fbf51a52bbc23243bf25ac21f4c2.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/280_b87378c9a789a14cb9a3f6914d054314.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/280_fdd55107bc403ac5c88613c752cf1ab0.jpg)
:quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/276_573cd9fea7326df557ebb2cb994e9001.png)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/206_6a5c643bacdc5c4f03e71fd82427116a.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/278_17c1bee0dcb2af4188ab87775d31d668.webp)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/50_1c3e5584d6e820404a829307ec5333fb.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/281_a22b1443b905f56da42292528d1fd6ce.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/153_5629abccd44d93110c510b8a3fdd6c2c.jpg)
Monden
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/233_cdf8546faa701e73479491916cee71d8.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/253_8b01cc75d6073696754903829a6c3e4c.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/197_a7c47440de52a491a53c2c047d9bacb8.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/274_15401aa4c567f156686109b016cd2212.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/284_374d69a5488f10e2ba0af40aded9b89d.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/16_d6b864931c55b91303c2f82871eb114e.jpg)
Politic
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/289_29f8c0145a3e11dc66cbef7ae35a07d2.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/206_a1e0d5d5ff1d69afdf8694a67b941b6a.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/255_c9646ad6c2d5657ee18465e364b372ab.webp)


:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2010/02/4315-227672-23spitalcantacuzino7.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/204_a0e9ae6e642bb266c61c2d9975556258.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/204_f81b3b9a7e86d7e3e1e841ac6b80a976.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/03/semn-interzis.jpg)
:quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/prognoza-meteo-minivacanta-1-mai.png)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/287_019e1f656eea5173e9752e19823f3789.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/287_47bf12ed48e0a94382090cb0ff3ca854.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/charlize-theron-apex-netflix.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/visuri-la-cheie.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/172_8de3158782b839fb2bcfebbee401487b.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/172_8fe71aa9667f28aefed1a0c0082f7e19.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/284_949001151d9ab4c0f8ded834648be536.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/275_46a15d920205618d75c06d5e86b47e30.jpg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/274_3301417cc8d77620dd4dcef656c734ed.jpeg)
:contrast(8):quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/179_cbccdf6838dc5c130e4415155bdd399e.jpg)
:quality(75)/https://www.libertatea.ro/wp-content/uploads/feed/images/179_246042b34857f66661de2bdd7c770f01.png)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/nicusor-dan-psd-aur-motiune-cenzura.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/toti-prefectii-subprefectii-si-secretarii-de-stat-psd-au-demisionat-inaintea-motiunii-de-cenzura-care-va-fi-votata-pe-5-mai-e1777449819480.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/01food.jpg)
:quality(75)/https://static4.libertatea.ro/wp-content/uploads/2023/04/mesaje-pentru-1-mai-1.png)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/prosop-sezlong-piscina.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/cartofi-fierti.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/garnituri-pentru-mici.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/barbat-face-mici-1-mai.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/fata-camp-stranut-batista.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/6838150971308826004758434926019552814299376n.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/ai-in-justitie--foto-ilustrativ-shutterstock2636798239-copy.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/radu-miruta.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2019/08/1-screenshot2019-08-28-strada-petricani-53.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/donald-trump-afp20260426a8z33khv4highreswhitehousecorrespondentsassociationdinner-copy.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/unite-state-russia-china-and-ukraine-on-chessboard-shutterstock2339727559-copy.jpg)
:contrast(8):quality(75)/https://static4.libertatea.ro/wp-content/uploads/2026/04/sorin-grindeanu-ilie-bolojan-id250029-inquam-photos-george-calin-copy.jpg)
Loghează-te în contul tău pentru a adăuga comentarii și a te alătura dialogului.